Crédits photo: ScenTree SAS
Si vous souhaitez référencer les produits de votre société ici,
merci de rentrer en contact avec l'adresse mail suivante fournisseurs@scentree.co pour en savoir plus sur nos offres dédiées aux annonceurs.
Si vous souhaitez référencer les produits de votre société ici,
merci de rentrer en contact avec l'adresse mail suivante fournisseurs@scentree.co pour en savoir plus sur nos offres dédiées aux annonceurs.
Général
-
N° CAS : 5137-52-0
-
N° EINECS : 225-895-7
-
N° FEMA : Donnée indisponible.
-
N° FLAVIS : 09.761
-
N° JECFA : Donnée indisponible.
-
Aspect : Liquide incolore
-
Densité : 0,982
-
Tenue : Coeur
-
Gamme de prix : €€
Physico-chemical properties
-
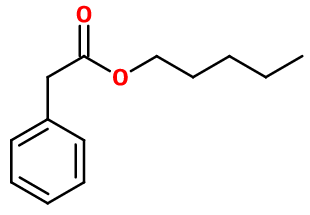
Formule brute : C13H18O2
-
Masse molaire : 206,28 g/mol
-
Log P : Donnée indisponible.
-
Point de fusion : Donnée indisponible.
-
Point d'ébullition : 269°C
-
Seuil de détection : Donnée indisponible.
-
Optical rotation : Donnée indisponible
-
Pression vapeur : Donnée indisponible
-
Indie de réfraction @20°C : Donnée indisponible
-
Valeur d'acide : Donnée indisponible.
-
Point éclair : 110°C
Utilisations
Utilisations :
Le Phénylacétate d'amyle est moins utilisé que le Phénylacétate d'isoamyle, il est tout de même utilisé dans des accords jacinthe, pour sa note à la fois rosée et verte, et pour faire le lien entre une tête verte et une note de cœur plus rosée.
Découverte :
Donnée indisponible.
Présence dans la nature :
Une trace de Phénylacétate d'amyle est présente dans la Menthe piperita HE. Il est donc possible d'en extraire à l'état naturel, en très faible quantité. C'est néanmoins la molécule synthétique qui est généralement utilisée en parfumerie.
Isoméries :
Le Phénylacétate d'amyle est un isomère de position du Phénylacétate d'isoamyle. Leur note est cependant assez différente : l'Isoamyl possède une note plus chocolatée, tandis que l'Amyl est plus vert et moins miellé. Le Floropal® est aussi un isomère de constitution de cette molécule. Il possède une note plus soufrée et fruitée, réminiscente de la rhubarbe.
Précurseurs de synthèse :
Le Phénylacétate d'amyle n'est pas précurseur de la synthèse d'un autre composé d'intérêt olfactif.
Voies de synthèse :
Comme la plupart des esters, le Phénylacétate d'amyle est synthétisé par une réaction d'estérification entre l'Acide Phénylacétique (obtenu à partir du chlorure de benzyl et du cyanure de sodium) et l'Alcool Amylique (ou Pentanol). Cette réaction est catalysée par un acide fort tel que l'acide sulfurique concentré, présent dans le milieu réactionnel en faible quantité. L'Acide Phénylacétique peut aussi être remplacé par de l'anhydride phénylacétique, pour augmenter le rendement de la réaction.
Réglementation & IFRA
Allergènes :
Cet ingrédient ne contient pas d'allergènes.
51ème amendement :
Cet ingrédient n'est pas réglementé par le 51ème amendement

